متانول با جرم مولکولی 42/32 در دسته الکلها با نامهای متیل الکل یا کربونیل، یکی از مهمترین مواد خام شیمیایی بوده و سومین ماده صنعتی پرمصرف جهان محسوب میشود.
تولید فعلی آن در ایران 39/3 میلیون تن در سال میباشد که در سال 1390 به 79/8 میلیون تن در سال خواهد رسید. 85% از تولید این ماده در صنایع شیمیایی بهعنوان ماده اولیه واکنش برای تولید فرمالدئید، اسید استیک و متیل ترشیوبوتیلاتر و یا بهعنوان حلال استفاده میشود ][1] و[2] [. امروزه یکی دیگر از مصارف رو به افزایش متانول، استفاده از آن بهعنوان سوخت میباشد ] [[3].
مهمترین واکنشهای صنعتی متانول عبارتنداز دهیدروژناسیون، کربونیلاسیون، استریفیکاسیون با اسیدهای معدنی یا آلی، اتری شدن، افزایش به بند دوگانه و جابجایی گروههای هیدروکسیل ][4] و[5][.
واکنش های تشکیل متانول از گاز سنتز(مخلوطCO، H2و مقدارکمی CO2) مطابق معادلات تعادلی زیر انجام میگیرد[6]] و[[7].

درحال حاضر، روش مرسوم برای اندازهگیری متانول در واحدهای صنعتی، ابتدا جداسازی دو فاز مایع و گاز و سپس اندازهگیری جداگانه مقدار متانول در هریک از فازها میباشد. بدین منظور ابتدا مخلوط را سرد کرده و سپس هر یک از دو فاز را جداگانه توسط دستگاه کروماتوگراف گازی آنالیز مینمایند ][8]، [9] و[10][. ولی در کارهای پژوهشی برای کم کردن خظا در جداسازی فازهای مایع و جامد بهتر است نمونه خروجی بهصورت یکجا آنالیز گردد. مهمترین پارامتر موثر در صحت آنالیز در دستگاههای کروماتوگرافی گازی، کالیبراسیون میباشد و با توجه به مشکلاتی که در راه کالیبراسیون مایعات در مخلوطهای گازی وجود دارد، بایستی شرایط را بهگونهای فراهم نمود که هر دو فاز تحت شرایط یکسان و تکرارپذیر به کروماتوگرافی گازی تزریق گردند.
نتایج فعالیتهای محققین نشان داده است که کالیبراسیون GC برای اندازهگیری متانول در مایعات مشکل چندانی نداشته و حتی میتوان مقادیر بسیاز ناچیز آن را با ساخت استاندارد در حد ppb اندازهگیری نمود ][11][، ولی ساخت مخلوط استاندارد گازی حاوی متانول مشکلات خاصی را بهدنبال دارد. از جمله روشهای متداول کالیبراسیون GC برای اندازهگیری مایع در گاز، میتوان به ساخت استاندارد مایع و تزریق میزان متناسب با حجم Loop [24]، استفاده از فاکتور پاسخ نسبی [[12]] و ساخت نمونه با استفاده از دو بمب شیشهای سپتومدار [[13]] اشاره نمود.
در تحقیق حاضر روش نوین کالیبراسیون دستگاه GC برای اندازهگیری متانول در مخلوطهای گازی با طراحی و راهاندازی Set-up آزمایشگاهی برمبنای رابطه کلازیوس-کلاپیرون ][14] و [15][ و یکی از مشتقات آن تحت عنوان معادله آنتوان ][16] و [[17]در فاز گازی، ابداع گردید. معادله آنتوان یک معادله فشار بخار بوده و رابطه بین فشار بخار و درجه حرارت را نشان میدهد.. در این روش ابتدا گاز نیتروژن در دماهای مختلف از متانول خالص عبور کرده و باتوجهبه معادله مذکور، فشار بخار جزئی متانول در مخلوط گازی اشباع بهدست آمد. همچنین با استفاده از معادله واندروالس ][18][ و گاز ایدهآل میتوان تعداد مولها و با اندازهگیری فشار کل و نسبت فشار جزئی به فشار کل، درصد مولی آن را نیز محاسبه و از این دادهها برای رسم منحنی کالیبراسیون دستگاه GC استفاده کرد.
در این مقاله، با توجه به تحقیقات انجام شده قبلی، روش جدیدی برای کالیبراسیون مایعات در گازها پیشنهاد و سیستم مربوط به آن ساخته شد. این سیستم یک کار ابتکاری و دارای تکرارپذیری زیادی بوده و مشکلات روشهای مرسوم را نیز ندارد. همچنین باتوجه به تائید شدن نتایج عملیات این کالیبراسیون با روشهای وزنی، میتوان ادعا نمود که این روش، بسیار موثر میباشد.
روش کار
ابتدا Set-up آزمایشگاهی، با استفاده از تجهیزات و قطعات مورد نیاز ساخته شده و سپس راهاندازی گردید که شمای کلی و PFD آن در شکلهای 1 و 2 نشان داده شده است.
بهمنظور انجام فاز عملیاتی، ابتدا جریان گاز حامل نیتروژن، پس از تنظیم و تثبیت سرعت جریان و عبور از یک کویل حرارتی مشابه با دمای حمام، به ظرفهای V1، V2 و V3 هدایت شد. جریان گاز ورودی با خوراک متانول برخورد کرده و پس از برداشته شدن گاز متانول اشباع، مخلوط گازی حاصل (نیتروژن و متانول) به سمت دستگاه GC هدایت شده و توسط یک شیر 6 راهه به دستگاه تزریق میشد. همچنین در طی عملیات فشار داخل لوله توسط فشارسنج مدل TC و دمای سیستم توسط سیرکولاتور کنترل میگردید. دادههای خام دستگاه GC که شامل سطح زیر منحنی بوده، پردازش و درصد مولی متانول به دو روش زیر محاسبه شد:
- بهدست آوردن فشار بخار متانول از معادله آنتوان در دمای حمام و فشار کل محیط (روش آنتوان).
- توزین گازشورها، قبل و بعد از آزمون و بهدست آوردن متانول مصرفی و تقسیم آن بر مجموع مولهای نیتروژن و متانول (روش وزنی).


روش آنتوان
معادله آنتوان ]30 و[19]] یک معادله فشار بخار بوده و رابطه بین فشار بخار و درجه حرارت را نشان میدهد.. این معادله از رابطه کلازیوس-کلاپیرون ][20]، [21] و[22][ مشتق شده است.

که در آن P: فشار بخار، T: درجه حرارت مطلق وA ، B و C ثابتهای معادله آنتوان هستند.
در این تحقیق، بهدلیل فاصله زیاد محدوده دمای کاری با نقطهجوش متانول، ضرورتی به استفاده از روابط با متغیرهای زیاد نبوده و فقط ضرایب معادله آنتوان را از مراجع معتبر استخراج و محاسبات مربوط به فشار بخار متانول انجام گردید ][23] و[24][. بهطوری که فشار بخار متانول با توجه به دمای حمام استخراج شده و سپس با توجه به فشار محیط (mmHg 652) و فشار موجود سیستم و با مدنظر قرار دادن قانون فشارهای جزئی، غلظت متانول برحسب mol% محاسبه شد.

روش وزنی
در این روش، ابتدا کلیه گاز شورها بههمراه متانول درون آنها وزن شده و سپس در مسیر جریان گاز حامل نیتروژن قرار داده شدند. بهطوری که جریان گاز N2 با سرعت جریان معینی که توسط دستگاه MFC کنترل میگردید، به مدت بیش از 24 ساعت از روی متانول عبور داده شده و جریان خروجی از گازشورها، به داخل GC و یا Vent هدایت میشد. در پایان، مجدداً کلیه گازشورها توزین و میزان متانول مصرفی، اندازهگیری میشد. در خاتمه با استفاده از کاهش وزن متانول، میزان درصد مولی آن بهکمک رابطه زیر (شماره 6) اندازه گیری شد.
 6
6
همچنین تعداد مول نیتروژن عبوری در طی این مدت با استفاده از معادله 7 بدست آمد:

با توجه به در دسترس بودن تعداد مول کل نیتروژن و متانول و همچنین ثابت بودن تغییرات غلظت متانول در نیتروژن در طی مدت فوقالذکر، درصد مولی متانول در نیتروژن با استفاده از معادله 8 محاسبه گردید.
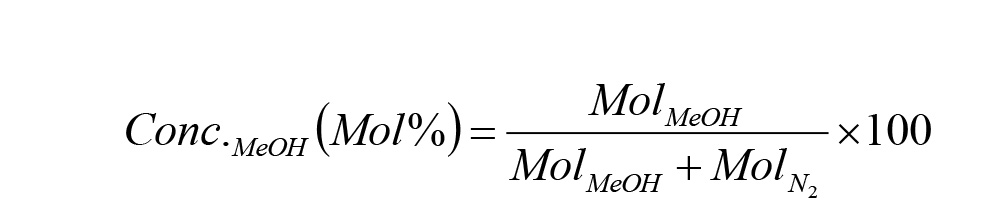
نتایج
مطابق بخش تجربی و باتوجهبه سیستم ابداعشده در شرایط دمائی 5، 0 و °C 5- و فشار محیط، پارامترهای نوع جنس رابطهای استفاده شده در ساخت Set-up، سرعت جریانی گاز نیتروژن، وجود یا عدم وجود تله (Trap) و زمان نمونهبرداری مورد بررسی قرار گرفت که در ادامه این بخش نتایج حاصل گزارش خواهد شد.
بهمنظور بررسی نوع جنس رابطهای استفاده شده در ساخت Set-up آزمایشگاهی روی تکرارپذیری نتایج، دو Set-up آزمایشگاهی مجزا با استفاده از شلنگهای سیلیکونی (شکل 3) و لولههای استنلس استیل (شکل 4) طراحی، نصب و راهاندازی گردید. سپس آزمایشات متعددی در دماهای مختلف اجراء شد که برای مقایسه، نتایج آزمونهای انجام شده در دمای oC 5- با دو رابط فوقالذکر در شکل 5 نشان داده شدهاست. بررسی نتایج تجربی نشان داد که مقادیر پارامترهای فوقالذکر حاصل از Set-up حاوی لولههای رابط استنلس استیل مناسبتر بوده و دادههای GC از تکرارپذیری قابلقبولی برخوردار هستند.


تاثیر سرعت جریانی گاز نیتروژن و وجود/یا عدم وجود تله
بهمنظور بررسی تاثیرپذیری میزان سرعت جریانی جریان گاز حامل N2 روی کالیبراسیون، در هر دمای مورد مطالعه، چهار سرعت جریانی مختلف 10، 20، 40و ml/min60 با قرار دادن یک و یا دو گازشور مورد مطالعه قرار گرفته و درصد مولی متانول با استفاده از معادله آنتوان محاسبه گردید. بدین منظور آزمایشات متعددی طراحی و اجراء شدند که آزمایشها نشان داد در صورت استفاده از تله، میزان انحراف نتایج از معادله آنتوان بسیار کمتر از حالتی است که در سیستم از تله استفاده نشود و همچنین سرعت جریانی بهینه گاز حامل نیتروژن، ml/min 40 میباشد.
بابک بزرگی، کارشناس ارشد آزمایشگاه کروماتوگرافی گازی شرکت پژوهش و فناوری پتروشیمی.
مراجع
[[1]] Shin-ichiro F.; Shuhei M.; Yoshinori K.; Miki K.; and Nobutsune T.; Applied Catalysis A: General; 207, 121-128; 2001.
[[2]] Breen, J.P.; Ross, J.R.H.; Catalysis Today; 51, 521-533; 1999.
[[3]] Kiler, R.; Chatika Voniy, V.; Herman, R.G.; Simmons, G.W.; J. Catal.; 74, 343; 1982.
[[4]] Monick, J.A.; Properties and Manufacture, Reinhold Publ. Co, New York, USA; 1986.
[[5]] Ferri, C.; Reaktionen der Organischen Synthese, Thicme Verlag, Stuttgart, Germany; 1978.
[[6]] Marschner, F.; Moeller, F.W.; Appl. Ind. Catal.; 2, 349-411; 1983.
[[7]] Chany, T.; Rousseau, R.; Kilpatrick, P.K.; Ind, Eng. Chen. Process. Des. Dev.; 25, 477; 1986.
[[8]] ASTM D-1945-03; Standard Test Method for Analysis of Natural Gas by Gas Chromatography.
[[9]] ASTM D 1722-98 (Reapproved 2004); Standard Test Method for Water Miscibility of Water-Soluble Solvents.
[[10]] ASTM E 346-99 (Reapproved 2003); Standard Test Methods for Analysis of Methanol.
[[11]] ASTM D 4307-99 (Reapproved 2004); Standard Practice for Preparation of Liquid Blends for Use as Analytical Standards.
[[12]] Heravi, J.; Fatemi J.M.H.; J. Chromatogr. A; 897, 227-235; 2000.
[[13]] HTAS 1131/E,No: 4136783 Rev.1
[[14]] Wark, K.; Generalized Thermodynamic Relationships; (5th ed.), New York, McGraw-Hill, Inc., USA; ISBN 0-07-068286-0; 1988.
[[16]] http://en.wikipedia.org/wiki/Antoine_equation
[[17]] Antoine C.; Comptes Rendus des Séances de l'Académie des Sciences; 107, 681-684, 778-780, 836-837; 1888.
[[18]] Gans, P.J.; Physical Chemistry Isolving van der Waals’ Equation; 1993.
[[19]] http://en.wikipedia.org/wiki/Antoine_equation.
[[20]] Wark, K.; Generalized Thermodynamic Relationships; (5th ed.), New York, McGraw-Hill, Inc., USA; ISBN 0-07-068286-0; 1988.
[[23]] http://www.s-ohe.com/Methanol_cal.html.
[[24]] Dortmund Data Bank